Oxit Nitric và Oxit Nito khác nhau như thế nào?
Nitric oxide và nitrous oxide là các phân tử của nitơ và oxy. Cả hai đều là chất khí trong khí quyển. Ngày nay, chúng được thải ra chủ yếu bởi các hoạt động của con người và ảnh hưởng đến môi trường theo những cách có hại.
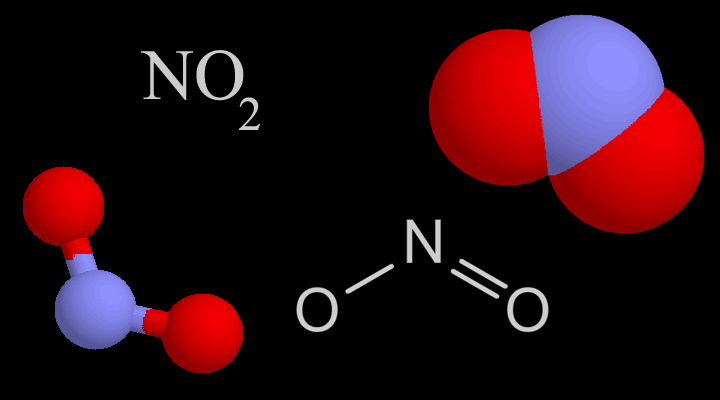
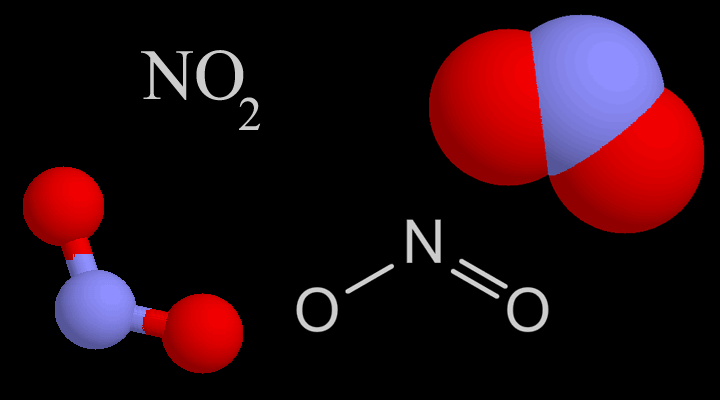
Oxit nitric và oxit nitơ là oxit của nitơ. Nitơ là một nguyên tố hóa học có số nguyên tử 7, và nó là một phi kim ở khối p của bảng tuần hoàn các nguyên tố. Nitơ trong các oxit khác nhau của nó có các trạng thái oxi hóa khác nhau. Trạng thái oxy hóa là số lượng electron mà một nguyên tử cụ thể có thể mất, đạt được hoặc chia sẻ với nguyên tử khác. Trong oxit nitric, nguyên tử nitơ chia sẻ hai electron với một nguyên tử oxy. Do đó, trạng thái oxi hóa của nitơ trong oxit nitric là +2. Ngược lại, trạng thái oxi hóa của nitơ trong oxit nitơ là +1. Đây là sự khác biệt chính giữa oxit nitric và oxit nitơ.
Oxit nitric
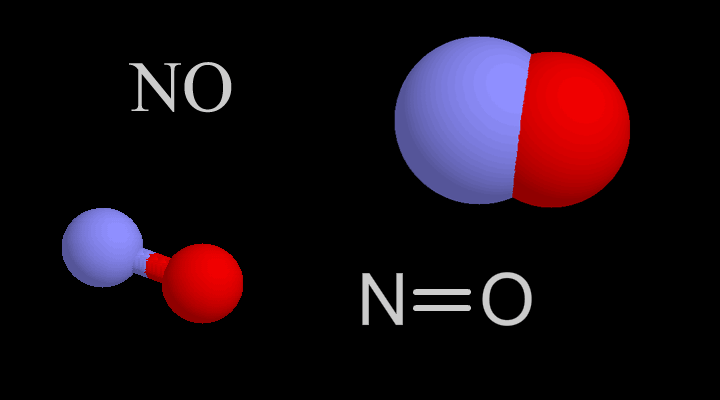
Oxit nitric là phân tử có công thức hóa học NO. Đây còn được gọi là nitơ monoxit. Đây là một gốc có một điện tử trên nitơ. Nitơ và oxy tạo ra hai liên kết cộng hóa trị giữa chúng. Đối với liên kết thứ ba giữa chúng, cả hai điện tử đều được tặng bởi nitơ. Do đó, nó là một liên kết âm. Oxit nitric có cấu tạo như sau.
Oxit nitric là chất khí không màu. Khi tiếp xúc với không khí, nó phản ứng với oxy, tạo ra khí nitơ đioxit có hại hơn nhiều. Oxit nitric là chất trung gian trong một số phản ứng hóa học. Nó được tạo ra như một sản phẩm phụ trong quá trình đốt cháy nhiên liệu hóa thạch trong động cơ xe và máy móc. Oxit nitric này có thể gây ra sự suy giảm tầng ôzôn cùng với nitơ điôxít. Đương nhiên, oxit nitric được tạo ra trong không khí khi ánh sáng xuất hiện. Trong quá trình này, nitơ và oxy trong khí quyển được kết hợp để tạo ra nitric oxide; đây là một bước quan trọng trong chu trình nitơ. Đây là nguồn nitrat để cung cấp dinh dưỡng cho cây trồng. Phản ứng như sau và nó là một phản ứng tỏa nhiệt.
N2 + O2 → 2 NO
Trong quá trình sản xuất oxit nitric thương mại, amoniac bị oxy hóa với sự có mặt của chất xúc tác bạch kim. Trong phòng thí nghiệm, khí oxit nitric được tạo ra khi cho kim loại đồng phản ứng với axit nitric. Trong các hệ thống sinh học, NO hoạt động như một chất khí báo hiệu.
Ôxít nitric có thể tạo thành nitơ điôxít khi có mặt ôxy. Nhưng trong nước, oxit nitric phản ứng với oxy và H2O để tạo thành axit nitơ (HNO2). Khi khí này được làm lạnh, nó tạo thành đime nitric oxit (N2O2). Đây là một số phản ứng chính của oxit nitric. Trạng thái oxi hóa của nitơ trong oxit nitric là +2. Đó là bởi vì, trạng thái oxy hóa của oxy là -2 và vì phân tử nitơ oxit là một hợp chất trung tính, trạng thái oxy hóa của nitơ nên là +2.
Nitơ oxit
Nitơ oxit là phân tử có công thức hóa học N2O. Đây là một loại khí không màu, không cháy và được gọi là khí cười hay khí ngọt. Cấu trúc của oxit nitơ có thể được vẽ như sau.
Vì một điện tích âm nằm trên một nitơ, nên cấu trúc cộng hưởng cho cấu trúc trên có thể được vẽ như sau.
Nitơ oxit được tạo ra bằng cách nung chất rắn amoni nitrat. Khí nitơ oxit được sử dụng trong phẫu thuật do tác dụng gây tê và giảm đau của nó. Hơn nữa, nó được sử dụng như một chất oxy hóa trong động cơ đốt trong. Ngoài ra trong động cơ tên lửa, chất này được sử dụng như một chất oxy hóa. Đây là một chất oxy hóa tốt ở nhiệt độ cao hơn. Ôxít nitric được tạo ra khi ôxít nitơ phản ứng với các nguyên tử ôxy, và điều này ảnh hưởng đến sự suy giảm tầng ôzôn. Vì vậy, đây được coi như một chất gây ô nhiễm không khí, sinh khí cho ngôi nhà xanh.
Điểm giống nhau giữa Nitric Oxide và Nitrous Oxide
Cả hai đều là chất khí không màu ở nhiệt độ và áp suất thường.
Cả hai đều được cấu tạo bởi các nguyên tử nitơ và oxy.
Cả hai đều là hợp chất cộng hóa trị.

Sự khác biệt giữa Nitric Oxide và Nitrous Oxide
Sự định nghĩa
Oxit nitric: Oxit nitric là một oxit của nitơ có công thức hóa học là NO.
Oxit nitơ: Oxit nitơ là một oxit của nitơ có công thức hóa học là N2O.
Khối lượng phân tử
Oxit nitric: Khối lượng mol của oxit nitric là 30 g / mol.
Oxit nitơ: Khối lượng mol của oxit nitơ là 44 g / mol.
Điểm nóng chảy và Điểm sôi
Oxit nitric: Điểm nóng chảy của oxit nitric là −164 ° C và nhiệt độ sôi là −152 ° C.
Oxit nitơ: Điểm nóng chảy của oxit nitơ là −90,86 ° C và nhiệt độ sôi là −88,48 ° C.
Tính nguyên tử
Oxit nitric: Nguyên tử của oxit nitric là 2.
Oxit nitơ: Nguyên tử của oxit nitơ là 3.
Trạng thái oxy hóa của nitơ
Oxit nitric: Trạng thái oxi hóa của nitơ trong oxit nitric là +2.
Oxit nitơ: Trạng thái oxi hóa của nitơ trong oxit nitơ là +1.
Nitric oxide là một chất gây ô nhiễm khí quyển đáng kể ở tầng thấp của bầu khí quyển. Nitơ oxit là một loại khí nhà màu xanh lá cây.
Ôxít nitơ có thể hình thành cấu trúc cộng hưởng, nhưng ôxít nitric thì không.
Ôxít nitơ được sử dụng cho mục đích y tế, nhưng ôxít nitric thì không.

Kết luận
Nitơ là một nguyên tố hóa học phi kim ở nhóm 5 của bảng tuần hoàn. Nó có thể tạo thành nhiều hợp chất oxit. Oxit nitric và oxit nitơ là hai hợp chất như vậy. Sự khác biệt chính giữa oxit nitric và oxit nitơ là nitơ của oxit nitric có trạng thái oxi hóa +2 trong khi trạng thái oxi hóa của nitơ trong oxit nitơ là +1.
Công Ty TNHH Khí Công Nghiệp Phú Thịnh chuyên nhập khẩu và phân phối các sản phẩm vỏ chai chứa khí, khí tinh khiết, khí công nghiệp, van giảm áp khí và các thiết bị sử dụng cho ngành khí.
